Elemen utama sebuah sel adalah protoplasma.
Protoplasma pada semua sel terdiri atas dua komponen utama, yaitu komponen anorganik dan komponen organik.
Komponen-komponen anorganik terdiri atas air, garam-garam mineral, gas oksigen, karbon dioksida, nitrogen, dan amonia, sedangkan komponen organik terutama terdiri atas karbohidrat, lipida, protein, dan beberapa komponen-komponen spesifik seperti enzim, vitamin, dan hormon (Sheeler & Bianchi, 1983). Pada sel hewan dan tumbuhan, protoplasma mengandung sekitar 75-85% air,
10-20% protein, 2-3% lipida, 1% karbohidrat, dan 1% zat-zat anorganik lainnya (De Robertis et al., 1975).
B. KOMPONEN ANORGANIK
1. Air
Di dalam sel, air terdapat dalam dua bentuk, yaitu bentuk bebas dan bentuk terikat. Air dalam bentuk bebas mencakup 95% dari total air di dalam sel. Umumnya air berperan sebagai pelarut dan sebagai medium dispersi sistem koloid. Air dalam bentuk terikat mencakup 4-5% dari total air di dalam sel (De Robertis et al., 1975).
Kandungan air pada berbagai jenis sel bervariasi diantara tipe sel yang berbeda. kandungan air (persen dari berat basah total) pada hati tikus, otot rangka tikus, telur bintang laut, E. coli, dan biji jagung secara berturut-turut masing-masing terdiri atas 6—72%, 76%, 77%, 73%, dan 13% (Sheeler & Bianchi, 1983). Air merupakan medium tempat berlangsungnya transpor nutrien, reaksi-reaksi enzimatis metabolisme sel dan transpor energi kimia (Lehninger, 1988).
Di dalam sel hidup, kebanyakan senyawa biokimia dan sebahagian besar dari reaksi-reaksinya berlangsung dalam lingkungan cair. Air berperan aktif dalam banyak
reaksi biokimia dan merupakan penentu penting dari sifat-sifat makromolekul seperti protein (Mayes et al., 1988). Air dan produk ionisasinya seperti ion O+ dan H-
sangat mempengaruhi berbagai sifat komponen penting sel seperti enzim, protein, asam nukleat, dan lipida. Sebagai contoh, aktivitas katalitik enzim sangat tergantung pada konsentrasi ion H+ dan OH- (Lehninger, 1988).
Oleh sebab itu, semua aspek dari struktur dan fungsi sel harus beradaptasi dengan sifat-sifat fisik dan kimia air.
Dari uraian di atas, dapat disimpulkan bahwa air merupakan komponen sel yang dominan dan berfungsi untuk :
a. Pelarut berbagai zat organik dan anorganik, misalnya berbagai jenis ion-ion, glukosa, sukrosa, asam amino, serta berbagai jenis vitamin.
b. Bahan pengsuspensi zat-zat organik dengan molekul besar seperti protein, lemak, dan pati. Dalam hal tersebut, air merupakan medium dispersi dari sistem koloid protoplasma.
c. Air merupakan media transpor berbagai zat yang terlarut atau yang tersuspensi untuk berdifusi atau bergerak dari suatu bagian sel ke bagian sel yang
lain.
d. Air merupakan media berbagai proses reaksi-reaksi enzimatis yang berlangsung di dalam sel.
e. Air digunakan untuk mengabsorbsi panas dan mencegah perubahan temperatur yang drastis di dalam sel.
Air mempunyai titik lebur, titik didih dan panas penguapan yang lebih tinggi dibandingkan dengan hampir semua cairan. Kenyataan ini menunjukkan
adanya gaya tarik yang kuat diantara molekul-molekul air yang berdekatan yang memberikan air gaya kohesi internal yang tinggi. Sebagai contoh, panas penguapan merupakan ukuran langsung dari jumlah energi yang dibutuhkan untuk mengalahkan gaya tarik menarik diantara molekul air yang berdekatan, sehingga molekul tersebut dapat saling berpisah dan masuk ke dalam fase gas.
Tabel Titik lebur, titik didih dan panas penguapan air dan beberapa pelarut lainnya (Lehninger, 1988).

Besarnya daya tarik antara dua molekul air yang berdekatan disebabkan karena setiap atom hidrogen menggunakan sepasang elektron secara bersama-sama
dengan atom oksigen sehingga menyebabkan atom molekul air berbentuk huruf V atau tetrahedral. Sisi oksigen yang berhadapan dengan dua hidrogen relatif kaya akan elektron, sedangkan pada sisi lainnya, inti hidrogen yang relatif tidak ditutupi membentuk daerah dengan muatan positif sehingga dikatakan bahwa molekul air bersifat dipolar atau dwikutub (Mayes, 1988; Lehninger, 1988) karena pemisahan muatan tersebut,
maka dua molekul air dapat tertarik satu dengan yang lainnya oleh gaya elek-trostatik diantara muatan negatif sebagian pada atom oksigen dari suatu molekul air dan muatan positif sebagian pada atom hidrogen dari molekul air yang lain. Jenis interaksi elektrostatik ini disebut ikatan hidrogen.
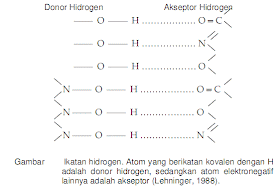
Ikatan hidrogen segera terbentuk antara atom yang bersifat elektronegatif, biasanya atom oksigen atau nitrogen, dan suatu atom hidrogen yang berikatan kovalen dengan atom elektronegatif lainnya pada molekul yang sama atau molekul lain. Atom hidrogen yang berikatan dengan atom elektronegatif kuat seperti oksigen cenderung mempunyai muatan positif kuat sebagian.
Akan tetapi, atom hidrogen yang berikatan kovalen dengan atom karbon yang tidak bersifat elektronegatif tidak berpartisipasi dalam pembentukan ikatan hidrogen.
2. Garam-garam Mineral
Kandungan garam-garam mineral pada berbagai tipe sel sangat bervariasi (tabel 2.2). Di dalam sel, garam-garam mineral dapat mengalami disosiasi menjadi anion
dan kation. Bentuk-bentuk anion dan kation tersebut dinamakan ion. Ion-ion dapat terlarut di dalam cairan sel atau terikat secara khusus pada molekul-molekul lain
seperti protein dan lipida. Secara umum, garam-garam mineral memiliki dua fungsi (Sheeler & Bianchi, 1983), yaitu :
a. Fungsi osmosis, dalam arti bahwa konsentrasi total
garam-garam terlarut berpengaruh terhadap pelaluan air melintasi membran sel;
b. Fungsi yang lebih spesifik, yaitu peran seluler setiap ion terhadap struktur dan fungsi dari partikel-partikel seluler dan makromolekul.
Berbagai jenis garam-garam mineral sangat penting untuk kelangsungan aktivitas metabolisme sel, misal-nya ion Na+ dan K+, berperan dalam memelihara tekanan osmosis dan keseimbangan asam basa cairan sel. Retensi ion-ion menghasilkan peningkatan tekanan osmosis sebagai akibat masuknya air ke dalam sel.
Beberapa ion-ion anorganik berperan sebagai kofaktor (tabel 2.3) dalam aktivitas enzim, misalnya ion magnesium. Fosfat anorganik digunakan dalam sintesis ATP yang mengsuplai energi kimia untuk proses kehidupan dari sel melalui proses fosforilasi oksidatif. Ion-ion kalsium dijumpai dalam sirkulasi darah dan di dalam sel. Di dalam tulang, ion-ion kalsium berkombinasi dengan
ion-ion fosfat dan karbonat membentuk kristalin. Fosfat dijumpai di dalam darah dan di dalam cairan jaringan sebagai ion-ion bebas, tetapi fosfat di dalam tubuh banyak terikat dalam bentuk fosfolipida, nukleotida, fosfoprotein,
dan gula-gula terfosforilasi (De Robertis et al., 1975).

Di dalam sel juga terkandung berbagai jenis gas yang berasal dari lingkungan atau dihasilkan oleh metabolisme sel. Beberapa gas yang terdapat di atmosfer dapat masuk ke dalam sel misalnya gas oksigen (O2), karbon dioksida (CO2), dan gas nitrogen (N2). Di dalam sel, oksigen berperan untuk mengoksidasi
bahan-bahan makanan. Karbon dioksida selain berasal dari lingkungan luar, juga dihasilkan dalam oksidasi bahan makanan sebagai hasil sampingan. CO2 dapat bereaksi dengan air membentuk asam karbonat yang selanjutnya mengalami disosiasi membentuk ion hidrogen dan bikarbonat dengan reaksi sebagai berikut :
C6H12O6 + 6 CO2 --------> 6 H2O + 6 CO2 + Energi
CO2 + H2O -------> H2CO3
H2CO3 ---------> H+ + HCO3-
Umumnya karbon dioksida di dalam sel berada dalam bentuk bikarbonat atau karbonat (Sheeler & Bianchi, 1983).

C. Komponen Organik
Komponen-komponen organik sel terdiri atas protein, lipid, karbohidrat, dan beberapa komponen-komponen spesifik lainnya seperti enzim, vitamin, dan
hormon. Lebih kurang 10-20% isi sel terdiri atas protein.
Protein merupakan makromolekul dengan berat molekul berkisar antara 10.000-10.000.000. sedangkan karbohidrat di dalam sel kurang lebih 1% dan umumnya dalam bentuk monosakarida, disakarida, dan oligosakarida, sedangkan lipida berkisar 2-3%. Masing-masing komponen organik sel tersebut akan dibahas secara terpisah pada uraian selanjutnya.
1. Protein
Protein adalah makromolekul yang terdiri atas asam-asam a-amino yang saling berikatan dengan ikatan kovalen diantara gugus a-karboksil asam amino dengan gugus a-amino dari asam amino yang lain. Ikatan di antara asam amino disebut ikatan peptida. Beberapa unit asam amino yang berikatan dengan ikatan peptida disebut polipeptida. Molekul protein dapat terdiri atas satu atau
sejumlah rantai polipeptida dan setiap rantai dapat terdiri atas ratusan hingga jutaan residu asam amino.
a. Klasifikasi
Hingga saat ini belum ada klasifikasi protein yang secara umum memuaskan. Klasifikasi protein yang menonjol didasarkan pada antara lain:
· Kelarutan
· Bentuk keseluruhan
· Peranan biologis
Pembagian protein juga dapat dilakukan berdasarkan fungsi dan strukturnya. Berdasarkan fungsinya, protein diklasifikasikan menjadi (i) protein enzim, berperan dalam mempercepat reaksi-reaksi biokimia, (ii) protein sruktural, membentuk struktur-struktur biologis, (iii) protein transpor, berperan sebagai
pengangkut subtansi-subtansi penting, dan (iv) protein pertahanan, melindungi tubuh dari invasi benda-benda asing. Berdasarkan strukturnya, protein diklasifikasikan menjadi: (i) protein globular, memi-liki pelipatan-pelipatan
yang kompleks, struktur tertier de-ngan bentuk yang tidak teratur. Protein serabut, meman-jang, lipatan sederhana,umum dijumpai pada protein struktural.
Dalam uraian berikut ini hanya dibahas klasifikasi berdasarkan bentuk dan peranan biologisnya. Berdasarkan bentuknya, protein dibagi menjadi :
1) Protein globular
Rantai polipeptida mengandung banyak lipatan dan berbelit. Rasio aksial kurang dari 10, misalnya insulin, albumin, globulin plasma, dan kebanyakan enzim.
2) Protein fibrosa
Rantai polipeptida atau kelompok rantai yang membelit dalam bentuk spiral atau heliks, dan dihubungkan oleh ikatan disulfida dan hidrogen. Rasio
aksial lebih besar dari 10, misalnya keratin dan miosin.

b. Ikatan-ikatan pada Struktur Protein
Struktur protein umumnya dipertahankan oleh dua ikatan sangat kuat yaitu ikatan peptida dan ikatan disulfida; dan tiga ikatan yang lemah, yaitu ikatan hidrogen, interaksi hidrofobik dan interaksi elektrostatif.
1) Ikatan peptida
Ikatan peptida adalah ikatan yang menghubungkan atom a-karboksil dari suatu asam amino dan atom a nitrogen dari asam amino yang lain.


Peptida yang dibentuk oleh dua molekul asam
amino disebut dipeptida; bila dibentuk oleh 3 molekul asam amino disebut tripeptida; dan bila dibentuk oleh banyak molekul asam amino disebut polipeptida.
2) Ikatan disulfida
Terbentuk antara 2 residu sistein yang saling berhubungan 2 bagian rantai polipetida melalui residu sistein.

3) Ikatan hidrogen
Terbentuk antara gugus NH- atau -OH dan gugus C=O dalam ikatan peptida atau -COO- dalam gugus R, misalnya dua peptida mungkin membentuk ikatan
hidrogen.

4) Interaksi hidrofobik
Rantai samping non polar asam amino netral pada protein cenderung bersekutu.
5) Interaksi elektrostatik
Merupakan ikatan garam antara gugus yang bermuatan berlawanan pada rantai samping asam amino.
c. Sifat-sifat Protein
1) Membentuk ion
Protein dalam air mampu membentuk ion + dan -,
dalam suasana asam membentuk ion positif dan dalam
suasana basa membentuk ion negatif.
2). Denaturasi
Denaturasi adalah perubahan konformasi alamiah menjadi suatu konformasi yang tidak menentu. Hal ini dapat terjadi karena terjadinya perubahan suhu, pH, atau terjadinya suatu reaksi dengan senyawa-senyawa lain misalnya ion-ion logam.
d. Asam Amino
Asam amino adalah asam karboksilat yang mempunyai gugus amino. Asam amino yang terdapat sebagai komponen protein mempunyai gugus NH2 pada
atom karbon a dari posisi gugus -COOH. Atom karbon a dari asam amino kecuali glisin masing-masing dihubungkan pada empat gugus kimia yang berlainan
sehingga atom karbon a bersifat asimetris. Oleh karena itu, molekul asam amino mempunyai dua konfigurasi yaitu D dan L.

Molekul asam amino dikatakan mempunyai konfigurasi L, apabila gugus NH2 di sebelah kiri atom karbon a. Bila gugus NH2 di sebelah kanan atom karbon
a, maka asam amino tersebut mempunyai konfigurasi D.
Struktur umum asam amino adalah:

Klasifikasi asam amino didasarkan atas:
pembentukannya di dalam tubuh dan strukturnya.
Klasifikasi asam amino berdasarkan pembentukannya di dalam tubuh ditunjukkan pada tabel

Asam amino esensial adalah asam amino yang tidak dapat dibuat dalam tubuh. Sedangkan asam amino non esensial adalah asam amino yang dapat dibuat
dalam tubuh.
Berdasarkan strukturnya, asam amino dikelompokkan menjadi 7 yaitu asam amino dengan rantai samping yang :
a. Merupakan rantai karbon yang alifatik, misalnya glisin, alanin, valin, leusin dan isoleusin.
b. Mengandung gugus hidroksil, misalnya serin dan threonin
c. Mengandung atom belerang, misalnya sistein, dan metionin
d. Mengandung gugus asam atau amidanya, misalnya asam aspartat, aspargin, asam glutamate, dan glutamine.
e. Mengandung gugus basa, misalnya arginin, lisin, hidroksilisin dan histidin
f. Mengandung cincin aromatic, misalnya
fenilalanin, tirosin dan triptofan.
g. Membentuk ikatan dengan atom N pada gugus amino, misalnya prolin dan hidroksi prolin
Uraian klasifikasi asam amino berdasarkan strukturnya diuraikan lebih detail pada pembahasan berikut. Beberapa rumus kimia asam amino adalah
sebagai berikut:


2. Karbohidrat
Molekul karbohidrat adalah substansi yang terdiri atas atom-atom C, H, dan O. Perbandingan antara molekul H dan O adalah 2:1. Jadi memiliki rasio yang sama dengan molekul air (H2O), misalnya:
Ribosa = C6H10O5
Glukosa = C6H12O6
Sukrosa = C12H24O11
Rumusa empiris dari karbohidrat adalah Cn(H2O)n.
Dengan dasar perbandingan tersebut, orang pada mulanya berkesimpulan bahwa dalam karbohidrat terdapat air, sehingga digunakan kata karbohidrat yang
berasal dari kata karbon dan hidrat atau air.

Karbohidrat sering disebut sakarida. Ada beberapa senyawa yang memiliki rumus empiris seperti karbohidrat tetapi bukan karbohidrat, misalnya C2H4O2 (asam asetat),
CH2O (formaldehida). Dengan demikian, senyawa yang termasuk karbohidrat tidak hanya ditinjau dari rumus empirisnya saja, tetapi yang penting adalah rumus strukturnya.
Dari rumus struktur, akan terlihat bahwa ada gugus fungsi penting yang terdapat pada molekul karbohidrat. Gugus fungsi itulah yang menentukan sifat senyawa tersebut. Berdasarkan gugus molekul yang ada pada karbohidrat, maka karbohidrat dapat didefenisikan secara kimia sebagai plohidroksialdehid atau polihidroksiketon serta yang menghasilkannya pada proses hidrolisis.
Berbagai senyawa yang termasuk kelompok karbohidrat mempunyai molekul yang berbeda-beda ukurannya, yaitu dari senyawa sederhana dengan berat molekul ren-dah hingga berat molekul besar. Berbagai senyawa terse-but dapat dibagi dalam empat golongan, yaitu monosaka-rida, disakarida, oligosakarida, dan
polisakarida.
a. Monosakarida
Monosakarida sering disebut gula sederhana (simple sugars) adalah karbohidrat yang tidak dapat dihidrolisis menjadi bentuk yang lebih sederhana lagi. Molekulnya hanya terdiri atas beberapa atom karbon saja.
Monosakarida dapat dikelompokkan berdasarkan kandungan atom karbonnya, yaitu triosa, tetrosa, pentosa, dan heksosa atau heptosa. Misalnya :
Triosa = (C3H6O3)
Tetrosa = (C4H8O4)
Pentosa = (C5H10O5)
Heksosa = (C6H12O6)
Monosakarida atau gula sederhana hanya terdiri atas satu unit polihidroksialdehida atau keton atau hanya terdiri atas satu molekul sakarida. Monosakarida yang umum dikenal mempunyai rumus empiris (CH2O)n, dimana n = 3 atau jumlah yang lebih besar lainnya. Kerangka monosakarida adalah rantai karbon berikatan tunggal yang tidak bercabang. Satu diantara atom karbon
berikatan ganda terhadap suatu atom oksigen membentuk gugus karbonil, masing-masing atom karbon lainnya berikatan dengan gugus hidroksil. Jika gugus karbonil berada pada ujung rantai karbon, monosakarida tersebut adalah suatu aldosa, dan jika gugus karbonil berada pada posisi lain, monosakarida tersebut adalah suatu ketosa. Berbagai jenis monosakarida aldosa dan ketosa
ditunjukkan pada gambar

Gambar Berbagai jenis monosakarida dalam bentuk aldosa (Frisell, 1982)
b. Disakarida.
Disakarida terdiri atas dua monosakarida yang berikatan kovalen terhadap sesamanya. Pada kebanyakan disakarida, ikatan kimia yang menggabungkan kedua unit monosakarida disebut ikatan glikosida, dan dibentuk jika gugus hidroksil pada salah satu gula bereaksi dengan karbon pada gula yang kedua.
Disakarida menghasilkan dua molekul monosakarida yang sama atau berbeda bila mengalami hidrolisis, misalnya:
Maltosa -------> Glukosa + Glukosa
Laktosa -------> Glukosa + Galaktosa
Sukrosa -------> Glukosa + Fruktosa
Oligosakarida menghasilkan 3-6 molekul monosakarida bila mengalami hidrolisis, misalnya :
Maltotriosa -------> 3 residu Glukosa
Rafinosa ---------> Galaktosa+ galaktosa + Fruktosa
Stakiosa ---------> Galaktosa + Glukosa + Fruktosa
c. Polisakarida
Polisakarida atau glikan tersusun atas unit-unit gula yang panjang. Polisakarida dapat dibagi menjadi dua kelas utama yaitu homopolisakarida dan
heteropolisakarida. Homopolisakarida yang mengalami hidrolisis hanya menghasilkan satu jenis monosakarida, sedangkan heteropolisakarida bila mengalami hidrolisis sempurna menghasilkan lebih dari satu jenis
monosakarida.
nice artikel
BalasHapus